
电话:029-87679000(总机)
地址:陕西省西安市西五路157号
邮编:710114
网址:www.2yuan.xjtu.edu.cn

电话:029-87679000(总机)
地址:陕西省西安市西五路157号
邮编:710114
网址:www.2yuan.xjtu.edu.cn



尊敬的患者朋友:
我院正在开展“评价JMT106注射液在晚期实体瘤参与者中的安全性、耐受性、药代动力学特征、免疫原性以及初步抗肿瘤活性的I期临床试验”。本研究药物JMT106注射液是由上海津曼特生物科技有限公司自主研发的以磷脂酰肌醇蛋白聚糖(Glypican3, GPC3)和干扰素-α (IFN-α)受体为靶点的双功能融合蛋白,为1类创新药。本研究已经获得国家药品监督管理局批准(批件编号:2025LP01343),已获得我院伦理委员会的批准。
一、药物介绍
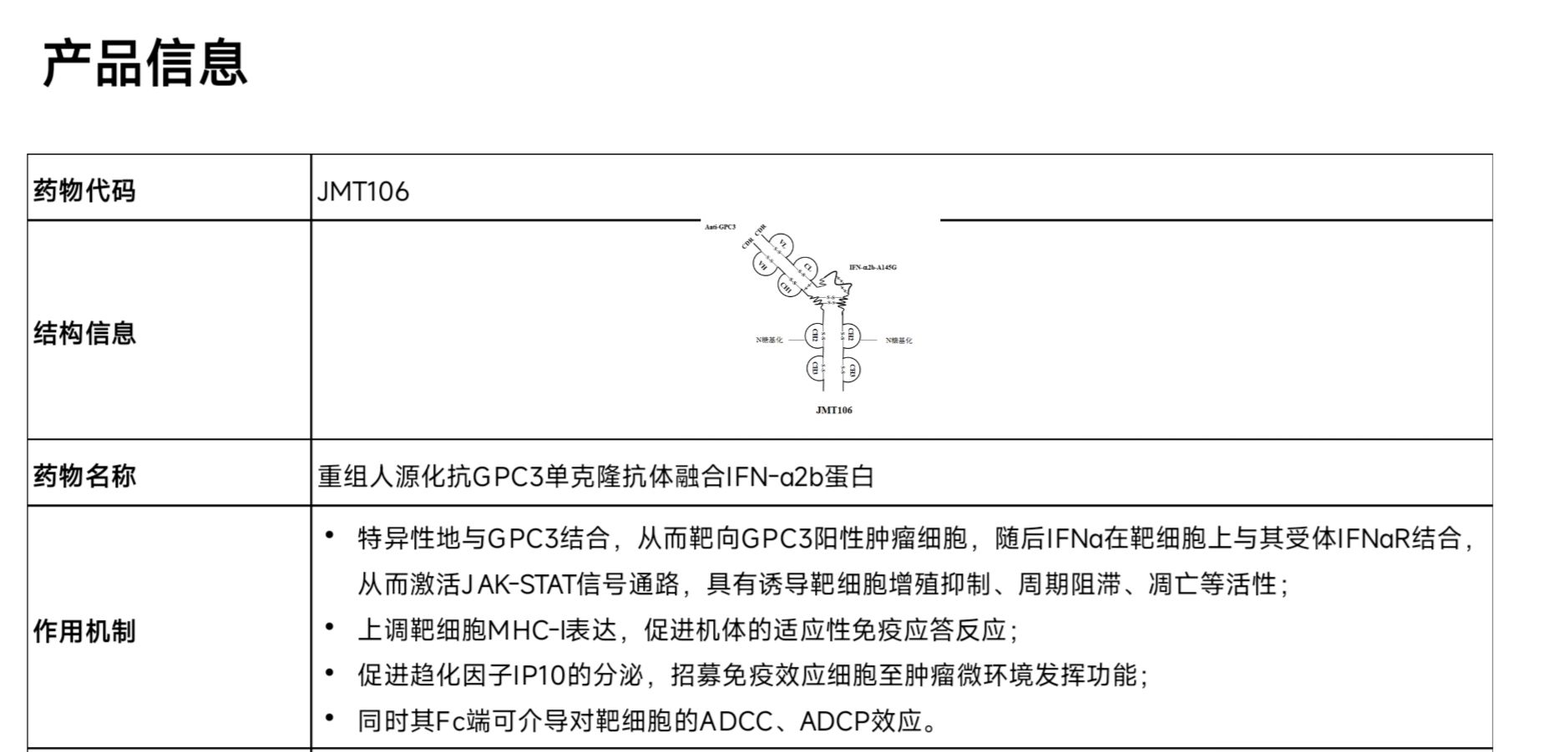
二、入排标准
1.参加本临床研究需要至少符合下列条件:
2.年龄≥18岁(获得知情同意时),性别不限且自愿签署知情同意书者;
3.组织学或细胞学诊断的晚期实体肿瘤参与者;
4.经至少一线标准治疗失败,或无标准治疗方案,或现阶段不耐受标准治疗;
5.根据RECIST v1.1,至少有一个可测量病灶;
6.ECOG体力评分0-1分。
希望了解具体情况的患者或者家属可与本试验相关负责医生联系,
最终是否入选由医生判定。
联系方式:
029-87678864/029-87678865
联系地址:
西安交通大学第二附属医院西门诊楼七楼东侧 I期临床试验研究病房